酸性雨発生のメカニズム
大気汚染のない自然の状態の雨でも、大気中の二酸化炭素が溶け込んでいるので弱酸性(pH5.6程度)を示しますが、pH5.0程度以下の雨を酸性雨と呼んでいます。
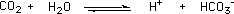
酸性雨発生のメカニズム
石油や石炭などの化石燃料中に含まれる硫黄分が、燃焼するとき二酸化硫黄(SO2)として発生します。
一方、自動車のエンジン内で、高温・高圧下で燃料が燃焼爆発するとき、大気中では通常起こり得ない以下の反応が起こり、一酸化窒素(NO)が生成します。

また、燃料自身に含まれる窒素分が高温で燃焼したときにも生成します。
こうして生じた排気ガスが、仮にゆっくり冷却された場合には、平衡が左に移動して窒素と酸素に分解されてしまうので問題はないのですが、実際には、高温の排ガスはエンジンから放出されるや否や、窒素と酸素に戻る間もなく急激に冷却されるので、一酸化窒素のまま大気中に大量に放出されます。
二酸化硫黄(SO2)も一酸化窒素(NO)も、大気中を拡散していく間に、徐々に酸化されて、それぞれ三酸化硫黄(SO3)、二酸化窒素(NO2)へと変化していきます。
こうして生じた硫黄酸化物(SOx)や窒素酸化物(NOx)は、雲の中の水滴に取り込まれたり、雨滴に溶け込んだりして、硫酸(H2SO4)・硝酸(HNO3)となり、酸性雨を作り出します。